Gelering van zetmeel
(Coachlab experiment)


|
Gelering van zetmeel |

|

|
Datum: Oktober 2011
Principe:
Door verhitten veranderd de structuur van het zetmeel.
Materiaal:
|
|
|
   |
Uitvoering:
|
|
|
|
|
|
 |
|
|
Microscopisch
onderzoek
|
|
Resultaat:
| Men kan op twee manieren
de temperatuur aflezen. Een manier is zoals onder is aangegeven. Kijken waar
er een afwijking optreedt in de lichtintensiteit en de corresponderende temperatuur
aflezen. In onderstaande geval ca. 66 °C. |
|
|
|
| Een tweede manier is door naar de eerste afgeleide
te kijken.
Deze berekenen we door twee opvolgende waardes van elkaar af te trekken zoals weergegeven in nevenstaande tabel. Vervolgens zet men de temperatuur, tijd en eerste afgeleide weer grafisch uit zoals weergegeven in onderstaande grafiek. De geleringstemperatuur kan men vervolgens aflezen door te kijken waar de
1ste afgeleide van de 0-lijn gaat afwijken. In dit geval ook weer bij ca. 66
°C. |
|
|
|
|
| De derde manier is om naar de tweede afgeleide
te kijken. We bepalen hiermee het buigpunt van een grafiek. Ook hier maken we weer een verschil berekening maar nu gebaseerd op het verschil tussen twee 1ste afgeleide waardes. Het buigpunt is nu dat punt waar een - waarde opgevolgd wordt door een + waarde en waar vervolgens het verschil het grootst is. Zie onderstaande grafiek. Het probleem hier is dat we een nogal ruizig signaal hebben, hetgeen het
niet makkelijk maakt om het buigpunt nauwkeurig te bepalen. Desalniettemin vinden
we ook hier een geleringstemperatuur nl. 66.4 °C. |
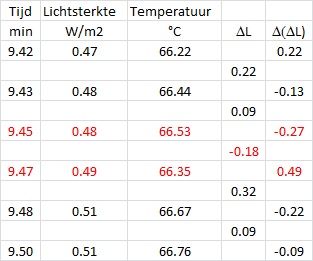 |
|
|
|
|
De meetresultaten zijn samengevat in onderstaande tabel. |
|
| Microscopisch onderzoek | |
 |
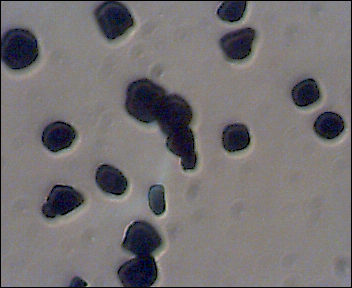 |
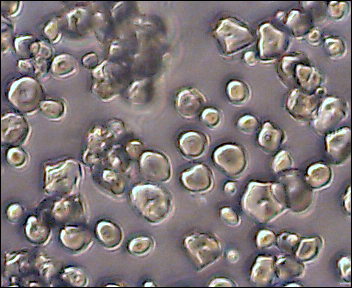
| Maiszetmeel (zonder joodkleuring) | Maiszetmeel (met joodkleuring) |
 |
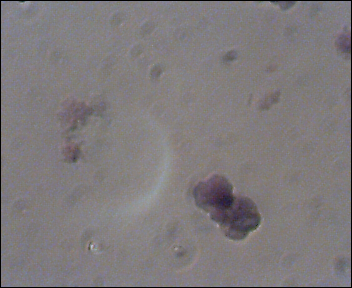 |
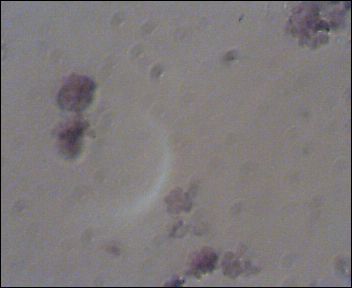
| Gegeleerd maiszetmeel (met joodkleuring) |
Gegeleerd maiszetmeel (met joodkleuring) |
| Het microscopisch onderzoek laat zien dat na gelering de zetmeelgranules als het ware opengebroken zijn, ze hebben een wazige structuur gekregen die moeilijk te zien is onder de microscoop. | |
Discussie:
| De twee meest belangrijke polysaccharides op zowel biologisch als economisch gebied zijn zetmeel en cellulose. Zetmeel is een hoog moleculaire polysaccharide (homopolysaccharide) day volledig afgebroken kan worden tot de individule glucose moleculen waaruit het is opgeboud door zure hydrolyse ( glucose = mono-saccharideeenheden). Zetmeel is opgebouwd uit 2 verschillende polymeren moleculen die in elkaar genesteld zijn nl. amylose en amylopectine. Amylose heeft een gemiddelde molecuulmassa van 106. Het is een polymeer van duizende glucose eenheden die aan elkaar gekoppeld via een a 1-4- binding aan elkaar gebonden zijn. Het amylose heeft een spiraalvormige structuur. Zetmeel is voornamelijk opgebouwd uit amylopectine dat een gecompliceerder, meer vertakte, structuur heeft. Het is niet opgebouwd uit duizenden glucose eenheden maar uit miljoenen glucose eenheden. De Glucose eenheden worden niet alleen maar gekoppeld via de 1-4 C atomen maar ook via het C 6 atoom. Vertakking treden elke 20 - 25 glucose eenheden waardoor het amylopectine een boomachtige structuur heeft. | |
|
De structuren van amylose
(lineair glucoseketen) en amylopectine (vertakte glucoseketen) |
|
| Verschillende van deze ketens worden door waterstofbruggen aan elkaar gebonden zodat zij aggregaten (korrels) vormen, de zetmeelkorrels genoemd, die onoplosbaar zijn in H2O. |
|
Wanneer zetmeel wordt
verwarmd in aanwezigheid van water worden de waterstofbruggen verbroken,
valt de ordening weg en wordt de zetmeel ook meer wateroplosbaar. Dit
irreversibele proces grijpt plaats bij de bereiding van voedingsmiddelen en
noemt men gelatinisatie. Gelatinering is een geleidelijk proces met
verschillende stadia: de granule zwelt, de oplosbare moleculen (in hoofdzaak
amylose) diffunderen uit de granule en de granule valt volledig uit elkaar.
Het resultaat is een zetmeelpasta die wel goed verteerbaar is. Het volledige
gelatinerings proces vindt dus niet plaats bij één welbepaalde temperatuur
maar over een welbepaald temperatuursbereik zoals aangegeven is in
nevenstaande grafiek. |
|
| Als men de oplossing laat afkoelen zonder te roeren vormt zich de gel. Bij afkoelen nemen de zetmeel moleculen weer een vaste vorm aan, de semi-kristallijne structuur die ze hadden voor verwarmen is echter verloren gegaan. Droogt men deze verkregen pap noemt men wordt het achtergebleven zetmeel nu stijfsel genoemd,. | |
Het microscopisch onderzoek bevestigd dat de meting met maïszetmeel is uitgevoerd. Uiteraard is dit niet verrassend aangezien we Maizena gebruikt hebben om dit experiment uit te voeren. |
|
|
|
|
Conclusie:
| Voor zowel maiszetmeel als stijfsel is een geleringstemperaturr van 66-67 °C bepaald, hetgeen overeenkomt met de waarden die men in de literatuur kan vinden. |
Opmerkingen:
|
Literatuur:
|
Relevante websites:
Minder relevante websites:
Achtergrondinformatie:
| Een gel is een oplossing in water van een sterk waterbindende stof die uit lange moleculen bestaat. De lange moleculen van de gel-vormende stof raken met elkaar verstrengeld, vooral als ze vertakt zijn, waardoor de vloeistof dik wordt. Door de sterk waterbindende eigenschappen, houden de gel-vormende molekulen veel water vast. De watermoleculen kunnen niet meer stromen en er ontstaat een soort pudding. Gelvormende stoffen worden veel gebruikt als verdikkingsmiddel in cosmetica en voedingsmiddelen. |
| Zetmeel |
|
Koolhydraten oftewel sacchariden, vormen een belangrijk bestanddeel in ons dagelijks voedsel en zijn vooral aanwezig in aardappelen, groenten, fruit, brood, melk, biet- en rietsuiker. Sacchariden zijn de belangrijkste bron van energie voor plant en dier. Meer dan de helft van onze dagelijkse opname aan sacchariden is zetmeel. Zetmeel is een reservekoolhydraat in planten en is een syntheseproduct van de fotosynthese. Zetmeel is vooral aanwezig in graangewassen (tarwe, rogge, rijst), vlinderbloemigen (bonen, erwten) en knolgewassen (aardappelen). Het eetbare deel van de aardappelplant is de knol. Die knol zit barstend vol zetmeel. Dit zetmeel is een energierijke verbinding die de plant eigenlijk had willen bewaren. Een plant spreekt zijn voorraad reservevoedsel aan als de fotosynthese niet mogelijk is.De industrie maakt dankbaar gebruik van zetmeel. Zetmeel is een koolhydraat en bestaat uit glucose eenheden die aan elkaar zijn gekoppeld tot een polymeer. Glucose is een zoetmaker. Daarom kunnen uit zetmeel, met behulp van enzymen (biologische katalysatoren), siropen worden gemaakt. Deze siropen kom je bijvoorbeeld tegen in frisdranken en vruchtensappen, in snoep en in bakkerijproducten. Het gebruik van stijfsel als plakmiddel berust op het verharden van stijfselpap bij verdamping van water. Het gebruik in linnengoed berust erop dat door de hitte bij het strijken een harde, glanzende laag dextrine ontstaat. Voor de bereiding van zetmeel gaat men meestal van aardappelen uit, die ongeveer 20% zetmeel bevatten. Ze worden fijngeraspt om de celwanden, die de zetmeelkorrels omsluiten, te verscheuren. De dusdanig verkregen massa wordt daarna met water op een zeef gespoeld, die de zetmeelkorrels doorlaat, maar de celwanden achterhoudt. Het zetmeel zet zich uit het water af en is na uitwassing en droging voor gebruik geschikt. Bij planten vindt in de mitochondriën alleen oxidatie van pyruvaat plaats. Pyruvaat ontstaat door afbraak van zetmeel (planten). Zetmeel worden eerst afgebroken tot glucose, dat vervolgens in de glycolyse wordt omgezet in pyruvaat. |
ZETMEEL |
| Andere naam: | Poly- Amylose |
| Molecuulformule: | HO-(C6H10O5)n-H |
| Structuurformule: |
![[ zetmeel ]](http://www.thuisexperimenteren.nl/science/zetmeel/zetmeel1.gif) |
25/12/2011