Oxaalzuur kristallen


|
Oxaalzuur kristallen |

|

|
Datum: Oktober 2015
Principe:
Materiaal:
|
|
Uitvoering:
|
Het maken van kristallen en een verzadigde oplossing |
|
|
 |
| Kristallen tussen diaraampjes | |
|
|
| Kristallisatie op objectglaasjes | |
|
   |
Resultaten:
|
Verzadigde oplossing met kristallen |
Diaraampje |
|
|
 |
| Objectglaasje | |
 |
|
| Microscopie | |
 |
 |
 |
 |
 |
 |
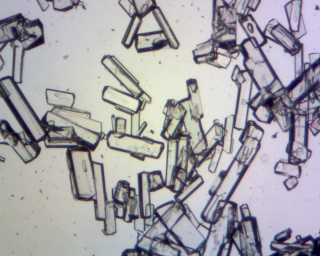
| Kristallen “gebroken” onder dekglaasje | |
 |
 |
| Zonder polarisatie | Met polarisatie |
Discussie:
|
Volgens de literatuur kristalliseert oxaalzuur met 2 moleculen
kristalwater uit in kleurloze naaldvormige kristallen hetgeen we in
bovenstaande experimenten inderdaad waargenomen hebben. Volgens de literatuur kristalliseert oxaalzuur in kleurloze zuilen, die bij gewone temperatuur aan de lucht niet veranderen, maar bij 100 °C hun kristalwater geheel verliezen en tot poeder uiteenvallen. |
Opmerkingen
|
Literatuur:
Relevante websites: |
Achtergrondinformatie:
Oxaalzuur is een reukloze
witte vaste stof. Oxaalzuur is een sterke dicarbonzuur. In de
analytische chemie wordt het gebruikt als analytisch reagens en algemeen
reducerend reagens. Oxaalzuur komt in tal van bladeren van planten voor.
Dit is van belang, omdat het calcium sterk bindt. Cruciferen hebben een
hoog calcium- en een laag oxaalzuurgehalte. Bij centrospermae en
Polygonalen is het omgekeerd het geval. Planten maken oxaalzuur aan om
zich te beschermen tegen vraat door insecten. De oxalaten zorgen voor
een onaangenaam gevoel van de tanden bij insecten waardoor de plant met
rust wordt gelaten. Een methode om oxaalzuur te maken is het verhitten van houtzaagsel met kaliumhydroxide. Er ontstaat
dan kaliumoxalaat, dat, opgelost in water met behulp van kalkmelk in
oxaalzure kalk wordt omgezet die in water onoplosbaar is. Door middel
van zwavelzuur maakt men vervolgens het oxaalzuur vrij. Dit is
gemakkelijk oplosbaar en oxaalzuur met 2 moleculen kristalwater
kristalliseert uit in kleurloze naaldvormige kristallen. |
||||
24/12/2015