Zwavel revisited


|
Zwavel revisited |

|

|
Datum: April 2018
Inleiding:
| In het verleden heb ik al eens een herkristallisatie uitgevoerd m.b.v. paraffineolie (lampenolie). Voor microscopisch onderzoek is dat echter iets minder geschikt. Recentelijk vond ik in de literatuur en op het web herkristallisaties uitgevoerd met tolueen en xyleen. Nu heb ik geen tolueen in mijn bezit maar thinner bevat xyleen. Het doel van dit experiment is om op een relatief snelle manier microkristallen geschikt voor microscopisch onderzoek te bereiden. |
Principe:
| Herkristallisatie van zwavel |
Materiaal:
|
|
|
|
Uitvoering:
Thinner heeft een nogal sterke geur. Voer dit experiment uit in een goed geventileerde ruimte. |
 |
|
|
|
Resultaten:
Kleine kristallen vormen
zich bijna onmiddellijk op het horlogeglas. |
Ook in de reageerbuis kan
men bij afkoelen kristalvorming waarnemen .  |
Het horlogeglas onder de binoculaire
microscoop. Foto genomen met telefoon op oculair.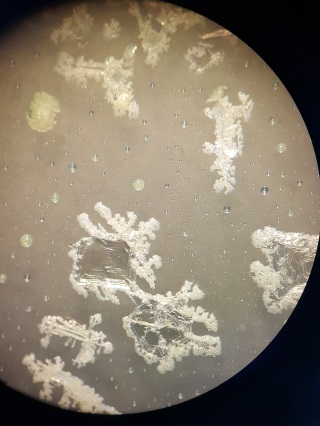 |
Opnames genomen met de DinoLite.
|
|
Opnames genomen met polarisatiemicroscoop en de LuckyZoom 5Mp camera. (gebruikte objectief onder foto) |
|
 Euromex Phase DM 20X / 0.40 DIN |
 Euromex Phase DM 20X / 0.40 DIN |
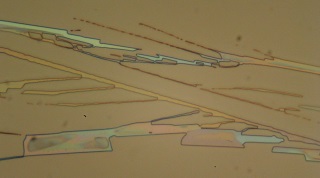 Euromex Phase DM 20X / 0.40 DIN |
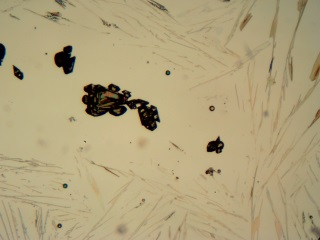 Euromex S. Flat Field 10 0.25 – 160 0.17 DIN |
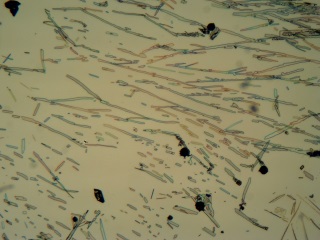 Meiji S. Flat Field 4/0.10 – 160 0.17 DIN |
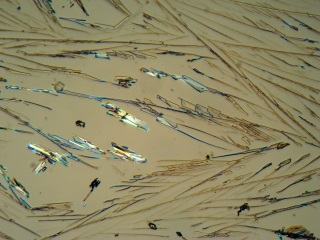 Meiji S. Flat Field 4/0.10 – 160 0.17 DIN |
 Meiji S. Flat Field 4/0.10 – 160 0.17 DIN |
 Meiji S. Flat Field 4/0.10 – 160 0.17 DIN |
Discussie:
| In dit experiment voeren we een herkristallisatie met thinner uit waarbij het amorfe zwavelbloem omgezet wordt in monokliene en (ortho)rhombische zwavelkristallen. | |
| Het zwavelmolecuul bestaat uit een achtring in zigzag vorm hetgeen in overeenstemming is met de sp3-hybridisatie van de zwavelatomen. |
|
| Het zwavelmolecuul bestaat uit een achtring in zigzag vorm hetgeen in overeenstemming is met de sp3-hybridisatie van de zwavelatomen. Zwavel komt in twee modificaties voor (beiden S8). Beneden 95.5 °C rhombisch en boven deze temperatuur monoklien. Bij 119.5 °C gaat de monokliene zwavel smelten waarbij een lichtgele beweeglijke vloeistof ontstaat, die nog steeds uit achtringen bestaat. De eigenschap dat er verschillende structurele vormen van hetzelfde element bestaan heet allotropie. | |
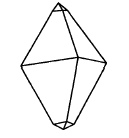 Typische vorm van rhombische zwavelkristallen |
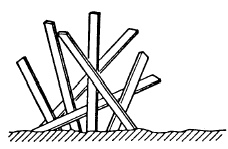 Typische vorm van monokliene zwavelkristallen |
|
Deze informatie helpt bij het verklaren van de visuele observaties die men maakt tijdens de uitvoering van dit experiment. In de reageerbuis kan men de vorming van kleine naaldvormige kristallen waarnemen hetgeen suggereert dat monoklien zwavel gevormd wordt. Deze observatie lijkt bevestigd te worden door de microscopische afbeelding waarbij het meren deel van de foto’s; naaldvormige kristallen laat zien. Slecht in enkele foto’s kan men rhombisch-achtige kristallen waarnemen (Figuur 6, Figuur 9 en Figuur 10). Deze observaties lijken contra-intuïtief te zijn als men bovenstaande gegevens in beschouwing neemt. De thinner met zwavel is echter opgewarmd naar een temperatuur boven 95.5 °C waar monokliene kristallen zich kunnen vormen. De oplossing werd vervolgens afgefiltreerd en, alhoewel de oplossing snel afkoelt, kunnen zich boven 95.5 °C monokliene zwavelkristallen vormen. Daarnaast zal de conversie van monoklien naar rhombisch zwavel enige tijd kosten en men kan aannemen dat door de snelle afkoeling de kristallen voornamelijk “bevroren” worden in hun monokliene vorm. Deze aanname lijkt bevestigd te worden als men het recept bestudeerd voor het maken van rhombisch zwavel. Zwavelbloem wordt opgelost in koolstofdisulfide en de herkristallisatie wordt uitgevoerd bij kamertemperatuur m.a.w. deze oplossing wordt niet verwarmd. Een interessant vervolg experiment kan zijn om deze preparaten gedurende langere tijd op te slaan en controleren of de conversie van monoklien zwavel naar rhombisch zwavel zich voortzet op het preparaat zelf. |
|
Literatuur:
|
Relevante websites |
Opmerkingen:
|
Achtergrondinformatie:
| Zwavel komt zowel in zuivere vorm als in de vorm van mineralen voor. In mineralen treft men zwavel aan als sulfide of sulfaat, gebonden aan mineralen. In het laboratorium zuivert men zwavel door een herkristallisatie uit te voeren met koolstofdisulfide, CS2. De kristallen die dan gevormd worden zijn echter vervuild met oplosmiddel, H2S en SO2. |
 Zwavel uit de El Desierto mijn in Potosi, Bolivia |
06/05/2018