Gefractioneerde destillatie op mikroschaal - revisited (CoachLab)


|
Gefractioneerde destillatie op mikroschaal - revisited (CoachLab) |

|

|
Datum: Januari 2025
Inleiding:
| Ik heb al eerder destillatie en gefractioneerde destillatie experimenten uitgevoerd met de microschaalkit maar was nooit echt tevreden met de destillatiecurven die ik produceerde. In het boek van de Jong vond ik een ietwat afwijkende proefbeschrijving en het leek me de moeite waard om die eens te proberen.. |
Materiaal:
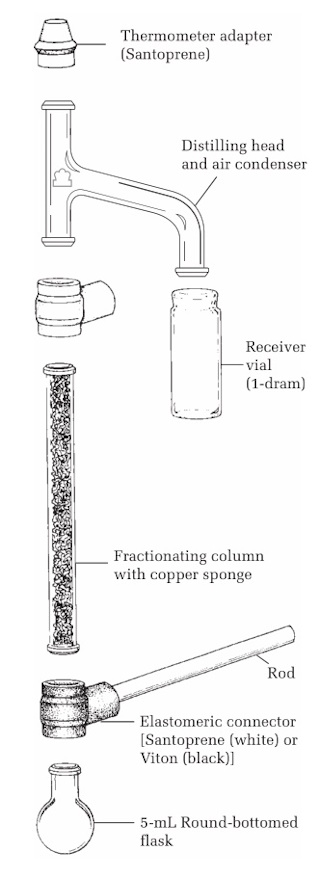
Microschaal kit met:
|
|
|
|
|
|
|
|
Uitvoering:
| Oplossing voor destillatie bereiden | |
Theelichtje
Stearine
|
|
 |
 |
| Vullen van de kolom met kopergaas | |
|
|
|
Destillatie |
|
|
 |
 |
|
Resultaten en discussie:
| Zoals ik in de inleiding vermeldde besloot ik dit experiment te herhalen na in het boek van de Jong een ietwat afwijkende proefbeschrijving te lezen. In de proef wordt een stukje kaarsvet opgelost in ethanol. De alcohol destilleert men over waarbij het kaarsvet moet achterblijven in de kolf. | |
| Men kan aan bovenstaande foto's zien dat het waxinemateriaal niet goed oplost, ook niet na toevoegen van een beetje wasbenzine. De stearine is echter wel goed oplosbaar in alcohol. Dit suggereert dat men met verschillende materialen te maken heeft. | |
| Onderstaande screenschots zijn van CoachLab, waarbij de grafiek eruit gelicht is. | |
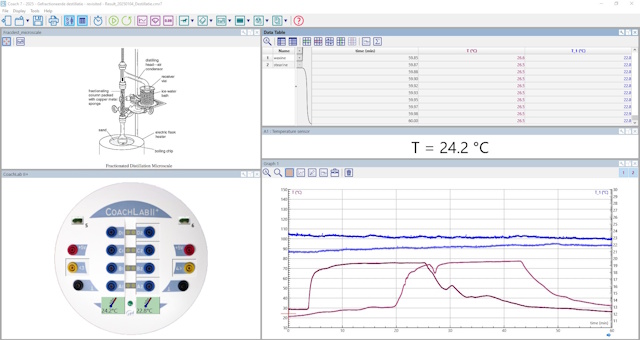 |
|
 |
|
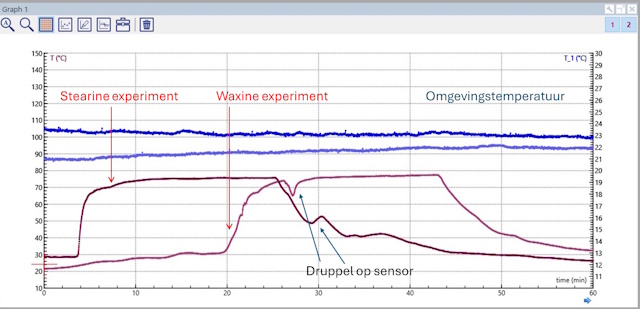
| Tot op heden had ik met deze microschaal opstelling altijd moeite om mooie destillatie curves te produceren. In dit geval is dat veel beter gelukt. | |
Toelichting op bovenstaande grafiek.
|
|
 |
 |
| Een video van de destillatie: | |
|
YouTube link: Gefractioneerde destillatie |
|
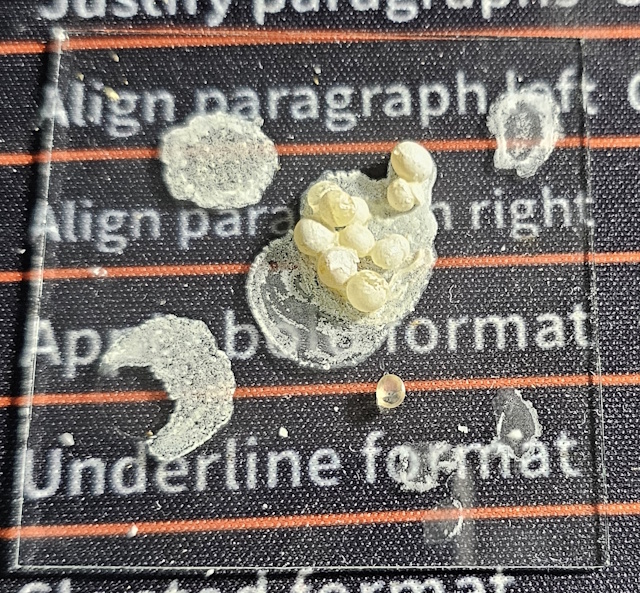
| Na afloop van de (stearine) destillatie heb ik de inhoud uitgegoten op een glasplaatje en laten drogen. Men kan wasresidue zien. | |
 |
|
| Ik dacht dat bij het eerste experiment met de waxine lichtjes helemaal geen materiaal opgelost was. Dat bleek bij schoonmaken van de kolf niet te kloppen. Zodra ik water toevoegde vormde zich een vetlaagje op de wand van de kolf die ik alleen met wasbenzine kon verwijderen. | |
|
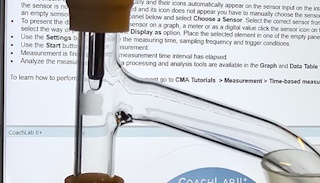
De vraag waar we het meest mee worstelen is waarom we een lagere kookpuntstemperatuur (ca. 75 °C) meten dan we verwachten (ca. 80 °C)? Ik vermoed dat het te maken heeft met een effect analoog aan de waargenomen druppelvorming op de sensor, die dan onmiddellijk tot een temperatuurdaling leidt. Ook als we geen druppelvorming zien kan zich nog altijd een filmlaagje vormen op de sensor die, doordat verdamping energie kost, zal bijdragen aan het waarnemen van een ietwat lagere temperatuur. |
|
Conclusies:
|
Opmerkingen:
|
Literatuur:
Relevante websites:
Minder relevante websites: |
|
Achtergrondinformatie: |
|
| De scheiding van een homogeen vloeistofmengsel door destillatie berust op het verschil in vluchtigheid van de bestanddelen. Dit laat zich het beste illustreren mbv een fasediagram waarbij het verband gegeven wordt tussen de temperatuur en de concentraties in de vloeistof- en dampfase voor een bepaalde totaaldruk. De kookpunten van de zuivere stoffen zijn A en B. | |
|
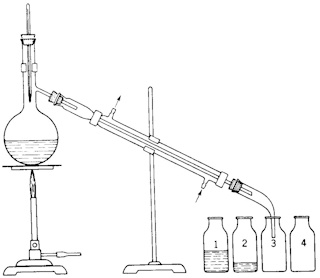
De curve AFDB geeft de kookpunten aan voor vloeibare mengsels van A en B (kookpuntslijn). De curve AEB geeft de samenstelling van de damp, die met de vloeistof bij een gegeven temperatuur in evenwicht is (dauwpuntslijn). Bij verwarming van een vloeistofmengsel C zal dit bij D beginnen te koken. De damp, die ontstaat heeft de samenstelling E en bevat meer van de vluchtige component dan de kokende vloeistof D. Koelt men deze damp af dan verkrijgt men destillaat F, waarin de concentratie van de meest vluchtige component groter is dan in het oorspronkelijke vloeistofmengsel C. De samenstelling van de kokende vloeistof zal tijdens de destillatie veranderen, hetgeen met een stijging van het kookpunt en een geleidelijke verandering van de samenstelling van de coëxisterende damp gepaard zal gaan. Men kan derhalve het destillaat in verschillende fracties opvangen en op deze wijze het meer vluchtige bestanddeel van het minder vluchtige scheiden. Deze manier van werken noemt men een gefractioneerde destillatie (Zie de tekening hier beneden). |
|
| Bij de zuivering door destillatie wordt een verbinding in dampvorm gebracht; de gevormde damp wordt daarna op een andere plaats gecondenseerd. Het kookpunt van een verbinding bij atmosferische druk is hoger dan het kookpunt bij een verminderde druk. Verbindingen, die bij verhoogde temperatuur snel ontleden, worden daarom bij voorkeur gezuiverd door destillatie onder verminderde druk. Indien de er een mengsel samenstelling is waarbij het kookpunt van dat mengsel beneden of boven het kookpunt van de individuele componenten ligt spreken we van een azeotropische samenstelling; bij deze samenstelling heeft de damp dezelfde samenstelling als de kokende vloeistof. Dergelijke mengsels kan men door destillatie niet verder scheiden. |
 |
|
Microschaal / microdestillatie set in
koffer. De set omvat de volgende onderdelen: |
|
|
|
|
|
|
09/01/2025