Zwavelkristallen


|
Zwavelkristallen |

|

|
Datum: Augustus 2013
Inleiding:
| Een van mijn redenen om met een microscoop aan de slag te gaan is omdat ik geïnteresseerd ben in microchemie en kristallen. Een experiment dat beide facetten combineert is het maken van zwavelkristallen. Indien men wel eens zwavelbloem onder een microscoop heeft bekeken dan ziet men nagenoeg geen kristallen. Om zwavelkristallen te maken moet men een herkristallisatie uitvoeren. |
Materiaal:
|
|
Uitvoering:
|
 |
Resultaten:
| Enkele observaties | |
 |
|
| Gesmolten zwavel | Opgelost zwavel |
| Op nevenstaande foto kan men al zien dat er min of meer naaldvormige zwavelkristallen neergeslagen zijn. |
 |
| Microscopisch onderzoek | |
|
Zwavelbloem 40 x Polarisatie microscoop
|
|
|
Zwavelbloem 100 x Polarisatie microscoop
|
 |
|
Zwavelkristallen 40 x Polarisatie microscoop
|
 |
|
Zwavelkristallen 100 x Polarisatie microscoop
|
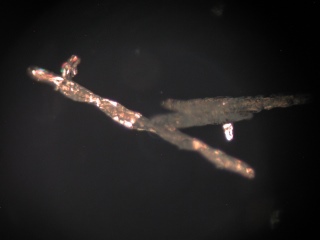 |
Discussie & Conclusies:
| Het zwavelmolecuul bestaat uit een achtring in zigzag vorm hetgeen in overeenstemming is met de sp3-hybridisatie van de zwavelatomen. |
|
|
Zwavel komt in twee modificaties voor (beiden S8). Beneden 95.5 °C rhombisch en boven deze temperatuur monoklien. Bij 119.5 °C gaat de monokliene zwavel smelten waarbij een lichtgele beweeglijke vloeistof ontstaat, die nog steeds uit achtringen bestaat. De eigenschap dat er verschillende structurele vormen van hetzelfde element bestaan heet allotropie. |
|
|
|
|
| Typische vorm van rhombische zwavelkristallen | Typische vorm van monokliene zwavelkristallen |
|
De microscopische opnamen van de zwavelbloem laten zien dat deze geen duidelijk herkenbare structuur hebben. Dat klopt ook aangezien zwavelbloem amorf is hetgeen betekent dat het geen structuur heeft. Nadat de herkristallisatie is uitgevoerd kunnen we wel een kristalstructuur waarnemen. Bij nadere beschouwing zien deze kristallen er naaldvormig uit, hetgeen de structuur is die we verwachten op basis van de literatuur |
|
Opmerkingen:
| In nevenstaande foto kan men het “droogkamertje” zien dat ik opgebouwd heb uit wat klemmen en wat “keuken” glaswerk. In deze opstelling kan men het zwavel laten drogen en toch enige bescherming tegen stof bieden. |
|
Literatuur:
|
Relevante websites:
Minder relevante websites:
|
Achtergrondinformatie: |
|
Zwavel komt zowel in zuivere vorm als in de vorm van mineralen voor. In mineralen treft men zwavel aan als sulfide of sulfaat, gebonden aan mineralen. Zwavel is een bestanddeel van insecticiden. Bij het vulkaniseren van rubber mengt men natuurrubber met zwavel en andere stoffen. Door verhitten vormt de zwavel verbindingen tussen de macromoleculen waaruit natuurrubber bestaat. De rubber behoudt zijn elastische eigenschappen, maar keert tevens tot zijn oorspronkelijke vorm terug. Vulkaniseert men met veel zwavel (30%), dan is het verkregen product hard en niet elastisch. Men noemt dit product eboniet. |
|
In het laboratorium zuivert men zwavel door een herkristallisatie uit te voeren met koolstofdisulfide, CS2. De kristallen die dan gevormd worden zijn echter vervuild met oplosmiddel, H2S en SO2. De beste manier om zwavel te zuiveren is door gebruik te maken van een verwarmingsbuis van kwarts die men verwarmd tot 700°C en onderdompelt in vloeibaar zwavel. De op koolstof gebaseerde verontreinigingen ontleden en vormen vluchtige verbindingen van vast koolstof die vastplakken aan de verwarmingsbuis. Na een week voert men nog een vacuümdestillatie uit hetgeen resulteert in zwavel met een koolstofgehalte van ca. 0.0009%. |
03/09/2013